近日,复旦大学生命科学学院王鹏飞青年研究员(通信作者)和复旦大学基础医学院姜世勃教授(通信作者)在免疫学权威杂志Nature Reviews Immunology(IF:108.555)上发表了关于针对SARS-CoV-2和其他人感染冠状病毒(HCoV)的广谱中和抗体(bnAbs)的综述文章“Broadly neutralizing antibodies to SARS-CoV-2 and other human coronaviruses” (doi: 10.1038/s41577-022-00784-3)。

这篇综述系统梳理了研究人员开发的各种针对新冠病毒(SARS-CoV-2)中和抗体,通过比较不同结合表位中和抗体的差异性,作者给出了选择中和抗体作为预防或治疗COVID-19的一些评价指标、并对抗体连用、改造抗体等后续研究方向给出了建议;此外通过分析中和抗体特性,利用反向疫苗学手段,作者还针对下一代广谱抗冠状病毒疫苗提出了研发策略。
自2019年新冠病毒出现以来,其多个变异株先后在全球部分地区主导一波疫情,造成数以百万计的死亡病例。并且新的变异株携带特定的突变更容易逃逸原有的免疫屏障,导致突破性(breakthrough)感染;一些已经获批临床或准备进入临床实验的中和抗体(nAb)也被证明其中和效果会被一些突变株抵抗,导致这些中和抗体失去原有的保护作用。
刺突(S)蛋白是冠状病毒的特征蛋白,主要负责与宿主细胞表面相应的受体识别并结合,帮助病毒进入宿主细胞。针对新冠病毒的中和抗体基本上也都是靶向S蛋白,尤其是S蛋白中的RBD(receptor-binding domain)区域。
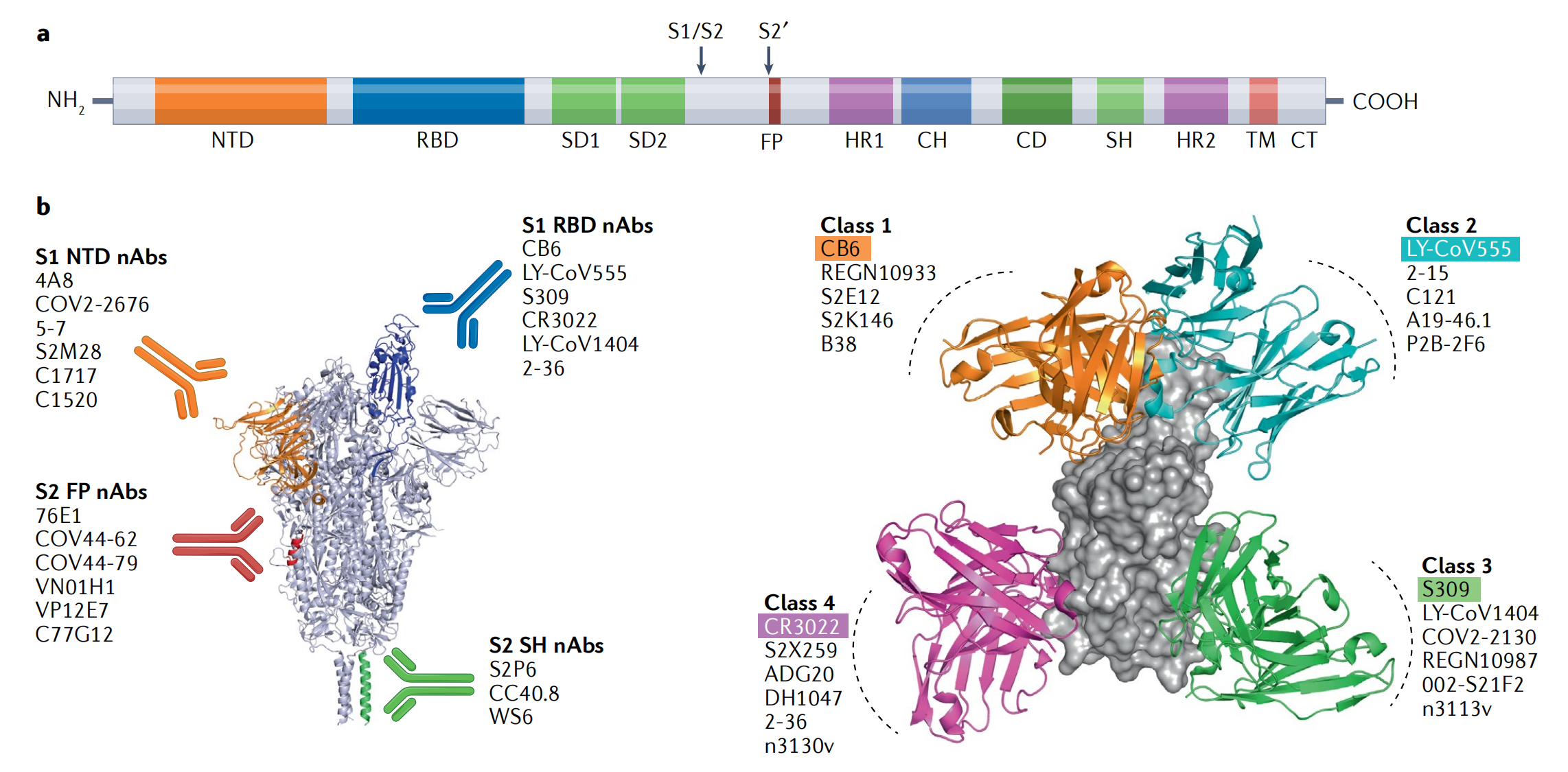
在这篇文章中,作者挑选了S蛋白上四个最常见的抗体表位:NTD(N-terminal domain)、RBD(receptor binding domain)、SH(stem helix)、FP(fusion peptide),通过查找已发表文章的中和抗体数据,按照抗体结合表位进行整理,在正文及补充材料的表格中,总结了超过60个单克隆抗体(mAb)的详细信息(主要包括:识别位点、中和机制、广谱程度和中和效率)

通过比较不同表位的中和抗体特征,作者发现那些针对NTD和RBD中class 1 & class 2的抗体因为识别的序列突变频率较高,很容易导致新病毒的免疫逃逸;而识别SH与FP的抗体,由于序列极高的保守性,这些抗体往往有着极好的抗冠状病毒广谱性。但作者同时指出,在筛选中和抗体用作预防或治疗COVID-19的药物时,要平衡抗体的中和效率与广谱性;或是连用不同表位的中和抗体/采用双特异性抗体或多特异性抗体,以期产生协同效应。此外,作者也提到针对现有的抗体,可以通过序列优化或是结构优化的办法产生更优性能的新抗体。
最后,针对疫苗设计,作者从保护广谱性角度出发,为下一代抗冠状病毒的疫苗设计给出两条指导建议:一是可以设计含有多种冠状病毒的S蛋白(完整或部分)抗原的疫苗,进行免疫接种,由于不同冠状病毒所含有的S蛋白(完整或部分)抗原存在序列上的差异,混合这些S蛋白,会增加机体免疫系统针对那些保守表位产生/增强免疫应答,并获得对应的记忆细胞的概率,起到广谱保护作用;二是挑选病毒表面蛋白中保守的免疫表位设计疫苗,并且联用高效佐剂,如基于STING 激动剂的新型佐剂——CF501,在免疫宿主体内诱生高效、广谱的中和抗体和T细胞免疫反应及防感染的保护作用。
复旦大学生命科学学院的陈彦嘉研究生、赵晓宇博士、纽约大学医学院(现在成都中医药大学)的周浩博士为论文的共同第一作者,复旦大学生命科学学院朱焕章教授参与了这篇综述的撰写。
获取原文/课题合作等,请联系王鹏飞青年研究员,邮箱:pengfei_wang@fudan.edu.cn

