复旦大学生命科学学院王陈继副研究员和同济大学附属第一妇婴保健院高昆研究员、万小平教授合作,于2022年12月9日在Cell Death & Differentiation杂志在线发表了题为“SPOP Mutations Promote Tumor Immune Escape in Endometrial Cancer via the IRF1–PD-L1 Axis ”的最新研究成果。
程序性细胞死亡受体1(PD-1)是一种重要的免疫抑制分子,为CD28超家族成员。以PD-1为靶点的免疫调节在抗肿瘤、抗感染、抗自身免疫性疾病及器官移植存活等方面均有重要意义。正常情况下免疫系统会对聚集在淋巴结或脾脏的外来抗原产生反应,促进具有抗原特异性的T细胞增生。程序性细胞死亡1配体(PD- L1)与PD-1结合,可以传导抑制性的信号,减低T细胞的增殖。肿瘤细胞逃避T细胞摧毁的一种途径是通过在它表面异常表达PD-L1识别PD-1后,传导抑制性信号,T细胞就不能发现肿瘤细胞和向肿瘤细胞发出攻击信号。PD-1/PD-L1阻断已发展成为癌症患者最有前途的免疫治疗策略之一,阻止PD-1和PD-L1的识别过程,部分恢复T细胞功能,从而使T细胞可以杀死肿瘤细胞。然而,导致肿瘤细胞中PD-L1异常过表达的遗传变异机制改变仍然知之甚少。
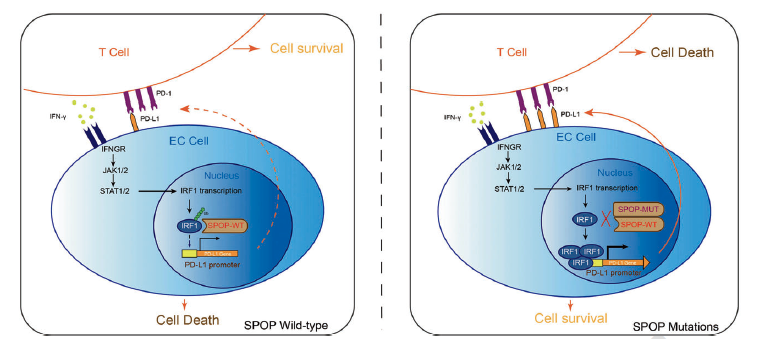
在内膜癌中,编码Cullin 3 E3泛素连接酶复合体底物识别亚基的SPOP基因存在高频突变(6-10%),但其突变导致内膜癌发生发展的分子机制仍不完全清楚。在本项研究中,该团队报道了SPOP可以在转录水平负向调节PD-L1。野生型SPOP结合IRF1,随后介导其泛素-蛋白酶体途径降解。由于IRF1是诱导PD-L1表达的主要转录因子,因此野生型SPOP可以抑制IRF1介导的PD-L1转录上调。相比之下,内膜癌来源的SPOP突变体失去了降解IRF1的能力、进一步上调了了IRF1和PD-L1表达。同时,内膜癌来源的SPOP突变体通过增加IRF1和PD-L1的表达来促进小鼠移植瘤的生长,且该促进作用可以被抗PD-L1单抗治疗所逆转。
本研究确定了SPOP作为IRF1-PD-L1轴的负调控因子,并描述了IRF1和PD-L1在SPOP突变驱动的内膜癌免疫逃避中的关键作用。另外,检测SPOP突变状态可能有助于识别对PD-1/PD-L1阻断免疫治疗有响应的内膜癌病人群体。
同济大学附属第一妇婴保健院的高昆研究员、复旦大学生命科学学院史晴博士后、同济大学附属第一妇婴保健院顾烨博士为该论文的共同第一作者。王陈继副研究员、高昆研究员和万小平教授为该论文的共同通讯作者。
原文链接:https://www.nature.com/articles/s41418-022-01097-7

