甘建华课题组合作解析首个SAM 依赖的甲基化核酶的晶体结构
2021年10月20日,国际期刊《Nature Catalysis》发布了本院甘建华课题组与生物医学研究院Alastair Murchie教授、陈东戎教授课题组合作的研究成果,标题为“The identification and characterization of a selected SAM-dependent methyltransferase ribozyme that is present in natural sequences”。
RNA甲基化在生物体内广泛存在,除核糖体RNA、转运RNA以及信使RNA外,甲基化同样存在于microRNA、snoRNA以及lncRNA等不同类型的RNA中,在蛋白质的翻译、基因沉默以及表观遗传过程中均发挥了关键作用。在生物体内,RNA甲基化通常由蛋白甲基转移酶催化,以体内普遍存在的腺苷甲硫氨酸(SAM)作为甲基供体,实现RNA特定位点的甲基化。
与蛋白质一样,很多RNA分子也具有催化功能,被称为核酶。目前,已有多种天然核酶被鉴定,参与生物体内多个关键的生物过程,包括核糖体催化的蛋白质酰胺键的形成,I类以及II类内含子的自我剪切反应等。运用人工筛选SELEX技术,研究者还发现了多种新型的RNA核酶,包括RNA甲基化核酶,然而已报道的甲基化核酶均以体内非常规的m6G或者m6PreQ1为甲基供体。
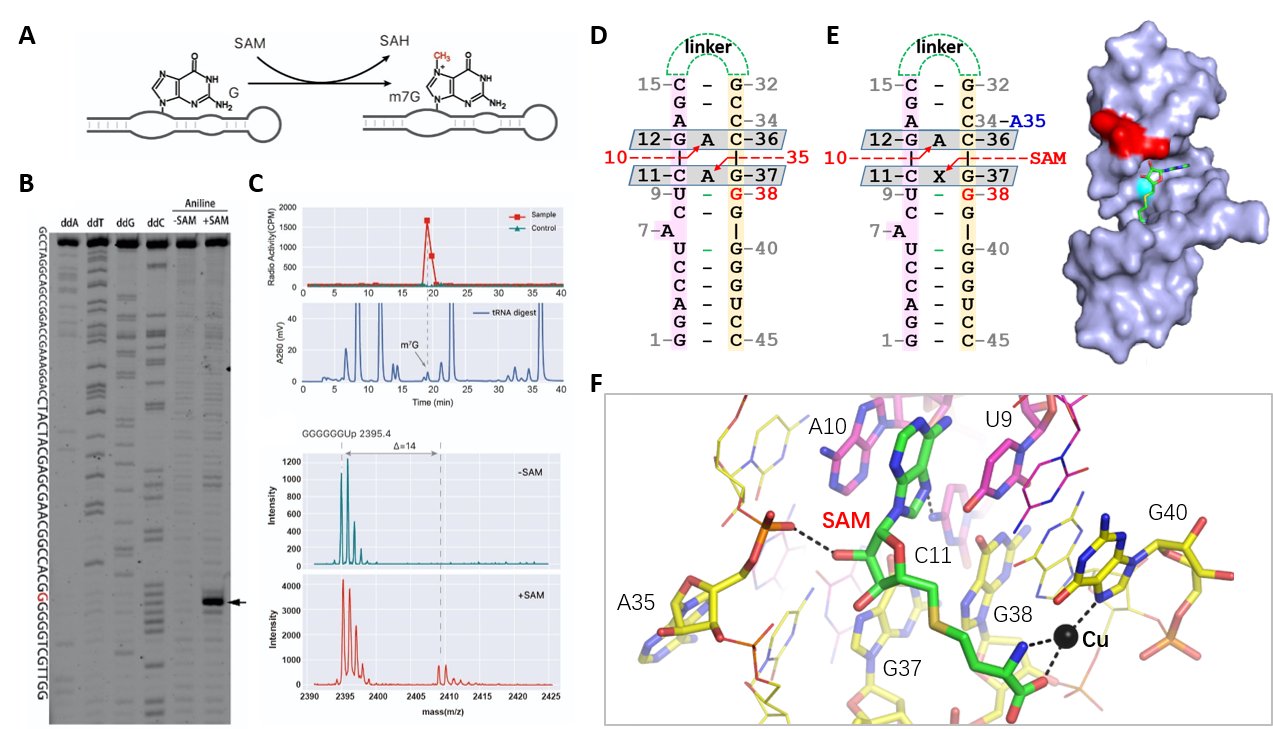
生物医学研究院的Alastair Murchie教授和陈东戎教授课题组运用SELEX技术,筛选获得了以SAM为供体的甲基化核酶,它可以催化鸟嘌呤N7位发生甲基化——一种在信使RNA的帽子结构普遍存在的RNA修饰。通过与Alastair Murchie和陈东戎教授合作,本院甘建华教授课题组解析了高分辨的RNA甲基化核酶的晶体结构。结构显示,该核酶具有两个“假三联体”碱基片层的堆叠。在加入SAM后,“假三联体”中的一个腺嘌呤发生翻转,形成结合口袋,识别SAM的腺嘌呤,而SAM的甲基则指向待催化的鸟嘌呤的N7原子,方便甲基的转移。联合结构分析和生物信息学搜索,Alastair Murchie教授和陈东戎教授还发现与该核酶类似的序列在生物体内广泛存在。目前,关于这些核酶类似序列的生物学功能正在进一步的深入研究之中。
该研究成果扩展了RNA作为催化剂的催化谱,演示了核酶能参与体内RNA甲基化以及调控生命过程的可能性,为RNA作为工具在表观转录层面调控生命过程提供了一个新的思路:以核酶精细调控RNA或者DNA的甲基化来进行基因表达的调控。
该研究主要由生物医学研究院助理研究员蒋恒义、本院博士后高延清共同完成,生物医学研究院张磊负责质谱检测实验,生物医学研究院的Alastair Murchie教授、陈东戎教授和本院甘建华教授为共同通讯作者。生物医学研究院周新文、张成为本研究提供质谱方面帮助,上海交通大学张薇指导完成DSC实验,上海同步辐射光源提供了X-射线衍射设施。
论文链接:https://www.nature.com/articles/s41929-021-00685-z

