复旦大学生命科学学院王陈继副研究员和上海市第一妇婴保健院高昆研究员合作,于2022年1月6日在Cell Death & Differentiation杂志在线发表了题为“SPOP mutations promote p62/SQSTM1-dependent autophagy and Nrf2 activation in prostate cancer”的最新研究成果。
自噬(autophagy)在真核细胞中高度保守,细胞通过它降解胞内组分,循环利用降解后的营养物质。自噬和泛素-蛋白酶体系统(UPS)是两种主要的蛋白质质量控制途径,长期以来被认为是相互独立的,然而最近的研究表明,这两个过程密切相关,并通过共同的泛素化信号相互调控。
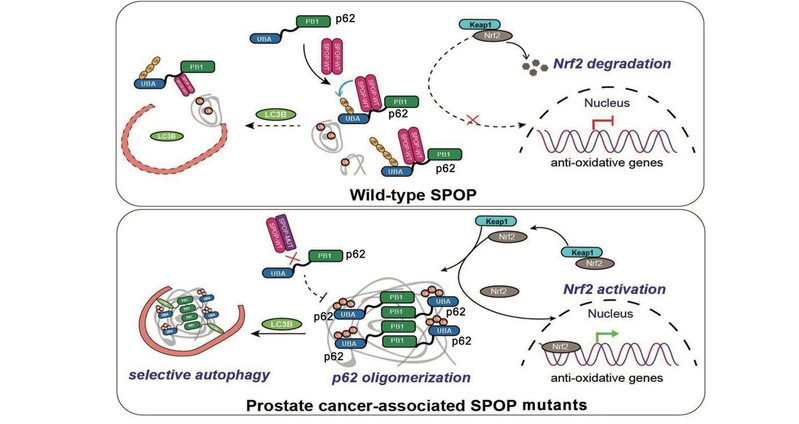
p62/SQSTM1是一个重要的选择性自噬受体,可驱动泛素化依赖性的自噬降解。同时该受体也是氧化应激信号的调控因子,通过激活Nrf2通路帮助细胞应对氧化应激。p62功能障碍与多种神经退行性疾病和癌症发生密切相关。尽管p62在病理生理上的重要性已被广泛认识,但人们对其在基础和应激条件下所受的动态调控仍未完全了解。在前列腺癌中,编码Cullin 3 E3泛素连接酶复合体底物识别亚基的SPOP基因存在高频突变,但SPOP突变导致前列腺癌发生的分子机制仍不完全清楚。该研究报道了细胞质定位的SPOP结合并介导p62UBA结构域K420位点的非降解型泛素化修饰。这种修饰作用降低了p62的泛素结合能力及其斑点形成和液相分离,从而抑制了p62依赖的自噬。此外,研究人员还发现SPOP可以抑制p62对Keap1的区隔作用,最终降低Nrf2对抗氧化基因的转录激活。而前列腺癌来源的SPOP突变体则失去泛素化p62的能力,并以显性负效应的方式促进自噬和氧化还原反应。该研究结果表明自噬和Nrf2激活在SPOP突变亚型前列腺癌的发生发展过程中具有重要作用,同时部分揭示了自噬和泛素-蛋白酶体系统之间的相互调控关系。
复旦大学生命科学学院博士后史晴、宁波大学副教授金晓峰、复旦大学医学院病理系章平肇副研究员和宁波大学医学院本科生李倩为该论文的共同第一作者。王陈继副研究员与高昆研究员为该论文的共同通讯作者。
原文链接:https://www.nature.com/articles/s41418-021-00913-w

