血吸虫病是由血吸虫感染引起的重要人畜共患病,全球约2亿人受影响。雌虫产生的大量虫卵既是主要致病因素,也是疾病传播的关键。血吸虫演化出独特的生殖模式——雌虫必须依赖雄虫持续合抱才能启动生殖发育,而雄虫分泌的信息素BATT被证实是这一过程的诱导信号,但其下游分子机制尚不清楚。
2026年3月6日,复旦大学王吉鹏研究员团队在 《Science Advances》 在线发表题为 “A male-pheromone-elevated transcription factor ZNF362.1 in female schistosomes determines sexual maturation” 的研究论文。该研究首次鉴定出雌虫的关键转录因子ZNF362.1,其能够感知雄虫分泌的信息素BATT信号,并同步激活卵巢与卵黄腺的发育程序。
研究团队通过转录组联合RNA干扰筛选,鉴定出BATT诱导雌虫性成熟的关键转录因子基因zinc finger protein 362(znf362)。该基因仅长转录本znf362.1发挥功能,其敲低完全阻断雌虫卵巢与卵黄腺分化,但不影响干细胞增殖,说明其调控干细胞分化而非维持(图1)。
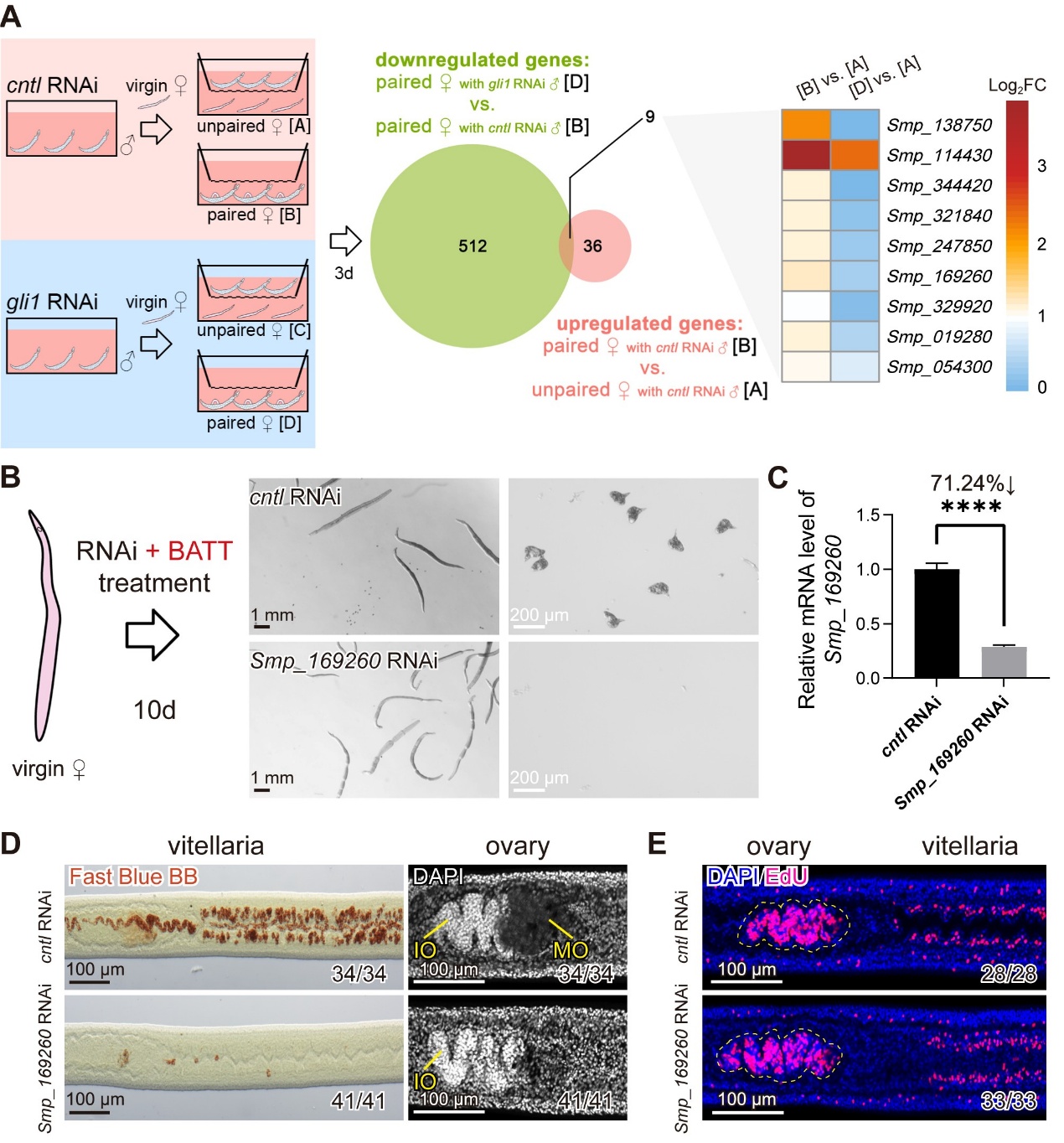
图1 BATT诱导雌虫生殖发育的关键基因
结合单细胞测序、DAP-seq与RNA-seq等多组学手段,研究团队发现znf362.1在BATT刺激后于虫体多数细胞中显著上调,并直接靶向cytoplasmic polyadenylation element binding protein 1(cpeb1)基因的启动子。cpeb1局限于卵巢和卵黄腺表达,其敲低表型与znf362.1一致,导致雌虫生殖发育受阻。qPCR、EMSA及双荧光素酶实验进一步确认,ZNF362.1能特异性结合cpeb1启动子并激活其转录。
深入解析其作用机制发现,CPEB1在卵巢与卵黄腺中呈现功能分化:在卵巢中,它通过调控cyclin B1 mRNA的poly(A)尾长度影响翻译,驱动卵母细胞减数分裂;在卵黄腺中,CPEB1虽同样高表达,但其调控S1细胞分化的路径不依赖于cyclin B1,提示其在不同组织中采用差异化的下游调控网络(图2)。
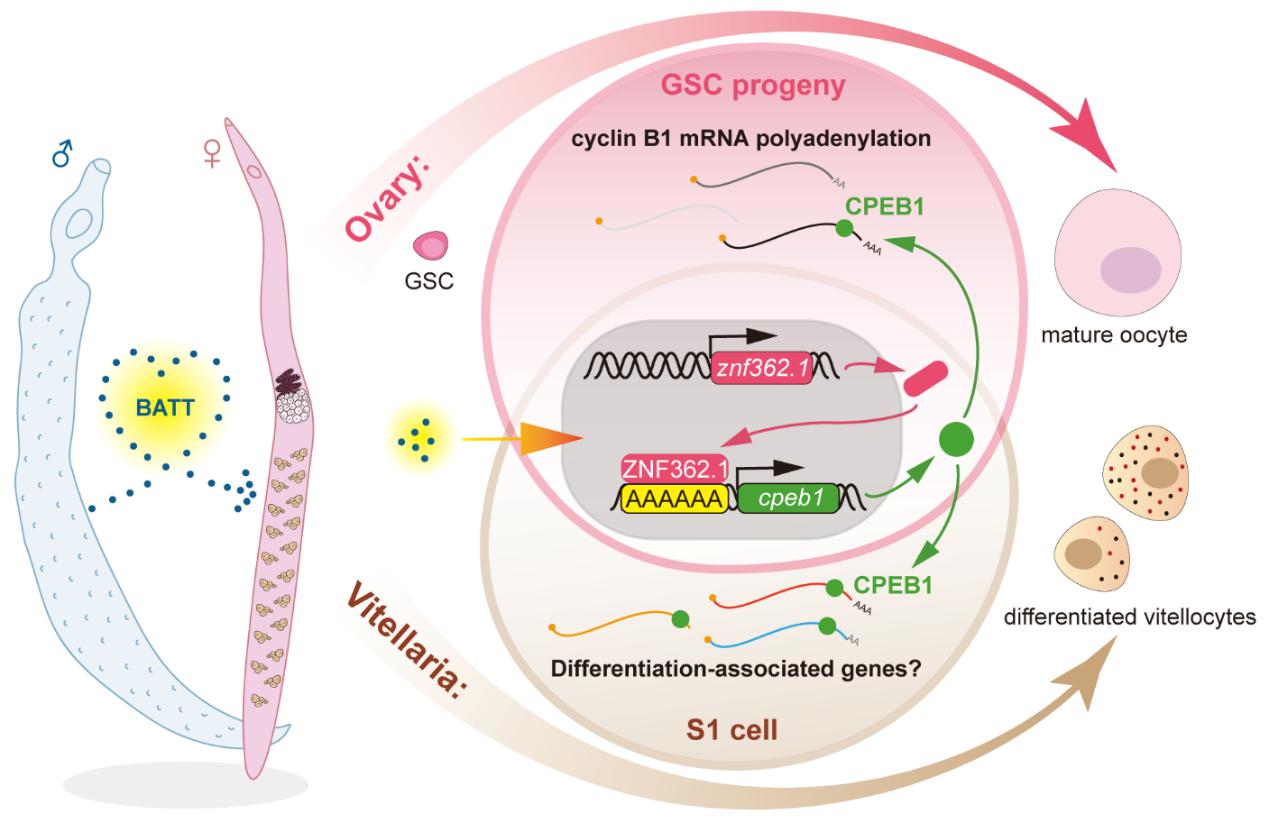
图2. ZNF362.1介导的血吸虫雌虫性成熟调控机制模型
本研究系统阐明了“BATT—ZNF362.1—cpeb1”信号轴调控雌虫性成熟的分子机制,并揭示了CPEB1在卵巢与卵黄腺中的差异化调控路径。该发现为理解血吸虫生殖调控提供了新视角,也为阻断虫卵传播的干预策略研发提供了理论支撑与潜在靶点。
复旦大学生命科学学院的王吉鹏研究员为该论文的通讯作者。复旦大学为第一完成单位。复旦大学生命科学学院博士研究生顾梦杰和程文君为该论文的共同第一作者。该课题受到国家重点研发计划、复旦曹娥江基础研究基金等项目的资助。
原文链接:
http://doi.org/10.1126/sciadv.aec6907

